مع استمرار تطور كوفيد-19 في الولايات المتحدة، يعمل الباحثون الآن على تطوير الجيل التالي من العلاجات، بما في ذلك نهج جديد يمكنه أن يساعد في تقليل الوقت اللازم للشفاء من المرض.
بينما تشتمل العلاجات الحالية على مضادات الفيروسات والأجسام المضادة والأدوية الستيرويدية، يركز العلماء في الولايات المتحدة وأوروبا الآن على إنشاء مستقبلات زائفة للمستقبلات التي يرتبط بها الفيروس عادةً؛ مما قد يبطل آثاره الضارة.
لتطوير العلاج الجديد، كان على العلماء أولاً تعديل الفئران بواسطة أحد أنماط البروتين البشري الذي يُعرف بالإنزيم المحول للأنجيوتنسين 2، أو ACE2. يتواجد هذا الإنزيم على سطح الخلايا ويساعد على تنظيم بعض الظواهر مثل الشفاء والالتهاب وضغط الدم.
وفي حين يمكن العثور على مستقبلات الإنزيم المحول للأنجيوتنسين 2 في كافة خلايا الجسم، إلا أنها تنتشر بشكل خاص داخل الرئتين والقلب والكلى والكبد، التي تعد هي الأعضاء التي يهاجمها المرض عادةً.
ولحماية مستقبلات الإنزيم المحول للأنجيوتنسين 2 الحقيقية، فيما يلي كيفية قيام المستقبلات الزائفة بعملها:
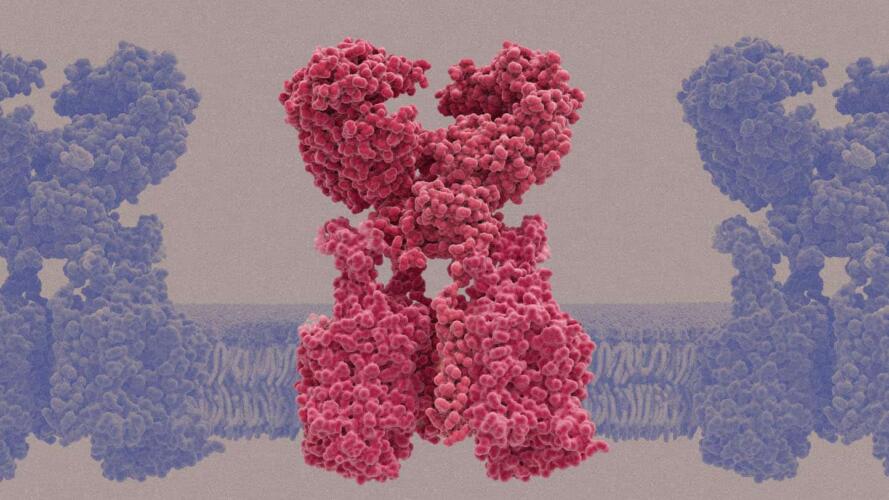
عادةً ما تلعب البروتينات الناتئة الموجودة على سطح الفيروس دور مفاتيح لمستقبلات الإنزيم المحول للأنجيوتنسين 2؛ ما يفتح الباب لدخول العدوى. لكن المستقبلات الزائفة، التي تُعطى عن طريق الوريد أو عن طريق الأنف -اعتماداً على مرحلة المرض- تعترض البروتين الناتئ وتحوّله بعيداً عن المستقبلات الحقيقية. وبعد الإصابة بالعدوى، يمكن أن يقلل العلاج من الحِمل الفيروسي داخل الجسم، ما قد يعني تماثل المرضى للشفاء بشكل أسرع.
في دراسة قادها دانييل باتل، أستاذ الطب في جامعة نورث وسترن، لم يظهر على الفئران التي أصيبت بالمرض وحصلت على العلاج سوى أعراض خفيفة فقط مقارنةً بالفئران التي لم تخضع للعلاج وتعرضت للموت.
حتى الآن، لا توجد سوى تجربة سريرية واحدة لمنتج يحتوي على الإنزيم المحول للأنجيوتنسين 2 قد اكتملت لدى المرضى الذين يعانون من أعراض متوسطة إلى شديدة. ومع ذلك، فإن عدداً أكبر من الباحثين يدعمون العلاج الجديد.
بدأ فريق باتل العمل على بروتينات المستقبلات الزائفة في يناير 2020 بعد اكتشاف أول حالة في الولايات المتحدة، وذلك بناءً على ما نعرفه من تفشي فيروس السارس في الصين عام 2003.
يقول باتل: "كنا نعلم أنه من المرجح جداً أن يكون مستقبل فيروس كورونا هو الإنزيم المحول للأنجيوتنسين 2؛ لأنه تبين في السابق أنه كذلك بالنسبة لفيروس السارس".
لكن تطبيق ذلك لم يكن بتلك البساطة؛ إذ يقارن مايكل جيويت، أستاذ الهندسة الكيميائية بجامعة نورث وسترن، والذي لم يشارك في الدراسة، بين عملية صنع المستقبلات الزائفة المعقدة وبين لعبة صعبة جداً لترتيب القطع لتشكيل صورة.
ويقول جيويت: "إن إعادة هندسة النظم البيولوجية المعقدة يمكن أن تكون أمراً صعباً. يمكن تشبيه الأمر بترتيب القطع لتكتمل الصورة وفي كل مرة تضع فيها إحدى القطع، تتغير باقي أجزاء الصورة".
ويقول جيويت أيضاً إنه بالمقارنة مع علاجات الأجسام المضادة، ينبغي أن تكون تكلفة المستقبلات الزائفة أقل واستخدامها أسهل. ويتفاءل بعض الخبراء بشأن قدرة المستقبلات الزائفة على منع السلالة الفيروسية الأصلية والطفرات القادمة.
وفي دراسة أخرى أجريت باستخدام عملية تسمى المسح العميق للطفرات، تمكن إريك بروكو، أستاذ الكيمياء الحيوية بجامعة إلينوي أوربانا شامبين، من مشاهدة آلاف الطفرات المختلفة للإنزيم المحول للأنجيوتنسين 2 في تجربة واحدة، ومعرفة أي منها يمكنها أن تجذب الفيروس وترتبط به بشكل أفضل. ثم قام فريقه ببناء مستقبلات زائفة تحاكي المستقبلات ذات الأداء الأفضل. لا ترتبط المستقبلات الزائفة بالخلايا ولكنها تعوم في السائل الموجود بينها للقبض على الفيروس قبل أن يرتبط بمستقبلات الإنزيم المحول للأنجيوتنسين 2 الحقيقية.
وعند الجمع بين ثلاث طفرات، تمكن فريقه من زيادة انجذاب فيروس كورونا للمستقبلات الزائفة بشكل كبير؛ إذ قاموا بإنتاج مستقبلات زائفة ترتبط بالفيروس بقوة أكثر 50 مرة من قوة الارتباط بالإنزيم المحول للأنجيوتنسين 2.
لاختبار هذا النهج، استخدم فريق بروكو أنسجة بشرية بدلاً من الحيوانات الحية. ويقول بروكو: "أصبحنا ندرك من خلال زراعة الأنسجة في المختبر أن بعض المستقبلات الزائفة تتمتع بنفس قوة الأجسام المضادة وحيدة النسيلة التي حصلت على الترخيص للاستخدام في حالات الطوارئ أو في التجارب السريرية؛ إذ إنها أفضل بقليل أحياناً، أو أقل فعالية بقليل في أحيان أخرى، ولكنها بشكل عام بنفس القوة".
يتمثل أحد المخاوف في أن إحدى هذه الطفرات قد تسمح بحدوث ما يسمى بالتفادي الفيروسي، وتساعد في تعزيز مقاومة الفيروس للعلاج. ولكن يقول بروكو إنه من غير المرجح أن يتطور الفيروس بشكل غير طبيعي نتيجة لعمل المستقبلات الزائفة لأنها تشبه المستقبلات الطبيعية إلى حد بعيد.
وبسبب الاختلافات في البنى التحتية والتعليم، فإن الوصول إلى تقنيات البيولوجيا التركيبية لا يتوزع بشكل متساو في جميع أنحاء العالم. ولا بدّ من إجراء المزيد من الأبحاث وتقديم المزيد من التمويل قبل توفير مثل هذا العلاج لعامة الناس. لكن مثل هذه التطورات قد تساعد في النهاية في التوصل إلى علاجات منخفضة التكلفة وقابلة للحمل وسهلة الاستخدام للمرض.
ويقول بروكو: "هناك علامات واعدة على أن المستقبلات الزائفة -التي تشبه مستقبلات الإنزيم المحول للأنجيوتنسين 2 البشرية إلى حد كبير- ستكون قوية وفعالة ضد كل تلك السلالات الجديدة. ولن أتفاجأ إذا وصل بعض من الجيل التالي من هذه المستقبلات الزائفة إلى العيادات في غضون عامين".